Corriente eléctrica en líquidos y gases.
Corriente eléctrica en líquidos.
 En un conductor de metal electricidad se forma por el movimiento dirigido de electrones libres y que no se producen cambios en la sustancia de que está hecho el conductor.
En un conductor de metal electricidad se forma por el movimiento dirigido de electrones libres y que no se producen cambios en la sustancia de que está hecho el conductor.
Dichos conductores, en los que el paso de una corriente eléctrica no va acompañado de cambios químicos en su sustancia, se denominan conductores de primera clase... Incluyen todos los metales, el carbón y una serie de otras sustancias.
Pero en la naturaleza también existen tales conductores de corriente eléctrica en los que se producen fenómenos químicos durante el paso de la corriente. Estos conductores se denominan conductores del segundo tipo... Incluyen principalmente diversas soluciones en agua de ácidos, sales y bases.
Si vierte agua en un recipiente de vidrio y le agrega unas gotas de ácido sulfúrico (o algún otro ácido o álcali), y luego toma dos placas de metal y les conecta cables, baja estas placas en el recipiente y conecta una corriente fuente a los otros extremos de los cables a través del interruptor y el amperímetro, luego el gas se liberará de la solución y continuará continuamente mientras el circuito esté cerrado.el agua acidificada es de hecho un conductor. Además, las placas comenzarán a cubrirse con burbujas de gas. Entonces estas burbujas se desprenderán de las placas y saldrán.
Cuando una corriente eléctrica pasa a través de la solución, se producen cambios químicos que dan como resultado la liberación de un gas.
Se denominan conductores del segundo tipo de electrolitos, y el fenómeno que se produce en el electrolito cuando una corriente eléctrica lo atraviesa es la electrólisis.
Las placas de metal sumergidas en un electrolito se denominan electrodos; uno de ellos conectado al polo positivo de la fuente de corriente se llama ánodo y el otro conectado al polo negativo es el cátodo.
¿Qué determina el paso de la corriente eléctrica en un conductor líquido? Resulta que en tales soluciones (electrolitos) las moléculas ácidas (álcalis, sal) bajo la acción de un solvente (en este caso agua) se descomponen en dos componentes y una parte de la molécula tiene una carga eléctrica positiva y la otra una uno negativo
Las partículas de una molécula que tienen carga eléctrica se llaman iones... Cuando un ácido, sal o álcali se disuelve en agua, se produce una gran cantidad de iones positivos y negativos en la solución.
Ahora debería quedar claro por qué pasó una corriente eléctrica a través de la solución, porque entre los electrodos conectados a la fuente de corriente, un diferencia de potenciales decir, uno de ellos resultó estar cargado positivamente y el otro negativamente. Bajo la influencia de esta diferencia de potencial, los iones positivos comenzaron a mezclarse hacia el electrodo negativo, el cátodo, y los iones negativos, hacia el ánodo.
Así, el movimiento caótico de los iones se ha convertido en un movimiento opuesto ordenado de iones negativos en una dirección y de iones positivos en la otra.Este proceso de transferencia de carga es un flujo de corriente eléctrica a través del electrolito y ocurre siempre que haya una diferencia de potencial entre los electrodos. A medida que desaparece la diferencia de potencial, la corriente a través del electrolito se detiene, el movimiento ordenado de los iones se interrumpe y el movimiento caótico comienza de nuevo.
Como ejemplo, considere el fenómeno de la electrólisis, cuando una corriente eléctrica pasa a través de una solución de sulfato de cobre CuSO4 con electrodos de cobre colocados en ella.
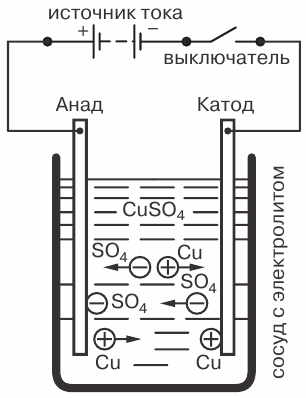
El fenómeno de la electrólisis cuando la corriente pasa a través de una solución de sulfato de cobre: C — recipiente con electrolito, B — fuente de corriente, C — interruptor
También habrá un movimiento inverso de iones a los electrodos. El ion positivo será el ion cobre (Cu) y el ion negativo será el residuo ácido (SO4). Los iones de cobre, al entrar en contacto con el cátodo, se descargarán (adjuntando a sí mismos los electrones que faltan), es decir, se convertirán en moléculas neutras de cobre puro y se depositarán sobre el cátodo en forma de los más delgados (moleculares). ) capa.
Los iones negativos que llegan al ánodo también son expulsados (donan el exceso de electrones). Pero al mismo tiempo, entran en una reacción química con el cobre del ánodo, como resultado de lo cual se agrega una molécula de cobre Cti al residuo ácido SO4, y se forma una molécula de sulfato de cobre CnasO4 y se devuelve de nuevo a la electrólito.
Dado que este proceso químico lleva mucho tiempo, el cobre se deposita en el cátodo, que se libera del electrolito. En este caso, el electrolito, en lugar de las moléculas de cobre que iban al cátodo, recibe nuevas moléculas de cobre debido a la disolución del segundo electrodo, el ánodo.
El mismo proceso ocurre si se toman electrodos de zinc en lugar de cobre, y el electrolito es una solución de sulfato de zinc ZnSO4.El zinc también se transferirá del ánodo al cátodo.
Por lo tanto, una diferencia entre la corriente eléctrica en los metales y los conductores líquidos radica en el hecho de que en los metales los portadores de carga son solo electrones libres, es decir, cargas negativas en electrolitos electricidad transportado por partículas de materia con carga opuesta: iones que se mueven en direcciones opuestas. Por eso se dice que los electrolitos tienen conductividad iónica.

El fenómeno de la electrólisis fue descubierto en 1837 por B. S. Jacobi, quien realizó numerosos experimentos para estudiar y mejorar las fuentes químicas de corriente. Jacobi encontró que uno de los electrodos colocados en una solución de sulfato de cobre, cuando una corriente eléctrica lo atravesaba, estaba recubierto de cobre.
Este fenómeno se llama electroformado, ahora encuentra una aplicación práctica extremadamente grande. Un ejemplo de esto es el recubrimiento de objetos metálicos con una fina capa de otros metales, por ejemplo niquelado, dorado, plateado, etc.
Corriente eléctrica en gases
Los gases (incluido el aire) no conducen la electricidad en condiciones normales. Por ejemplo, una meta alambres para lineas aereasal estar suspendidos paralelos entre sí, están aislados entre sí por una capa de aire.
Sin embargo, bajo la influencia de altas temperaturas, una gran diferencia de potencial y otras razones, los gases, como conductores líquidos, se ionizan, es decir, en ellos aparecen partículas de moléculas de gas en grandes cantidades que, como portadores de electricidad, contribuyen al paso. de una corriente eléctrica a través del gas.
Pero al mismo tiempo, la ionización de un gas difiere de la ionización de un líquido conductor.Si la molécula se divide en dos partes cargadas en un líquido, entonces en los gases bajo la acción de la ionización, los electrones siempre se separan de cada molécula y el ion permanece en forma de una parte cargada positivamente de la molécula.
Solo hay que detener la ionización del gas, ya que deja de ser conductor, mientras que el líquido sigue siendo siempre conductor de corriente eléctrica. Por lo tanto, la conductividad del gas es un fenómeno temporal, que depende de la acción de causas externas.

Sin embargo, hay algo más tipo de descarga electricaLlamado descarga de arco o simplemente arco eléctrico. El fenómeno del arco eléctrico fue descubierto a principios del siglo XIX por el primer ingeniero eléctrico ruso V. V. Petrov.
V.V. Realizando numerosos experimentos, Petrov descubrió que entre dos carbones conectados a una fuente de corriente, aparecía en el aire una descarga eléctrica continua, acompañada de una luz brillante. En sus escritos, V.V. Petrov escribió que en este caso "la calma oscura puede iluminarse de manera suficientemente brillante". Así, por primera vez se obtuvo luz eléctrica, que fue prácticamente aplicada por otro ingeniero eléctrico ruso, Pavel Nikolayevich Yablochkov.
"Svesht Yablochkov", cuyo trabajo se basa en el uso de un arco eléctrico, hizo una verdadera revolución en la ingeniería eléctrica en ese momento.

La descarga de arco se utiliza hoy en día como fuente de luz, por ejemplo, en proyectores y dispositivos de proyección. La alta temperatura de la descarga del arco permite que se utilice para dispositivos de horno de arco… Actualmente, los hornos de arco accionados por corriente muy alta se utilizan en una serie de industrias: para la fundición de acero, hierro fundido, ferroaleaciones, bronce, etc. Y en 1882, NN Benardos utilizó por primera vez la descarga de arco para cortar y soldar metales.
En tuberías de gas, lámparas fluorescentes, estabilizadores de voltaje, para obtener haces de electrones e iones, la llamada descarga de gas incandescente.
Descarga de chispa Se utiliza para medir grandes diferencias de potencial utilizando un espacio de chispa esférico, cuyos electrodos son dos bolas de metal con una superficie pulida. Las bolas se separan y se les aplica una diferencia de potencial medible. Luego, las bolas se acercan hasta que pasa una chispa entre ellas. Conociendo el diámetro de las bolas, la distancia entre ellas, la presión, la temperatura y la humedad del aire, encuentran la diferencia de potencial entre las bolas según tablas especiales. Con este método, es posible medir con una precisión de un pequeño porcentaje una diferencia de potencial del orden de decenas de miles de voltios.
