Dieléctricos polares y no polares
De acuerdo con los puntos de vista de la física clásica, los dieléctricos son fundamentalmente diferentes de los conductores, porque en condiciones normales no tienen cargas eléctricas libres. La carga total de las partículas que forman moléculas dieléctricas es cero. Sin embargo, esto no significa en absoluto que las moléculas de estas sustancias no sean capaces de exhibir propiedades eléctricas.
Todos los dieléctricos lineales conocidos se pueden dividir en dos grandes grupos: dieléctricos polares y dieléctricos no polares. Esta división se introduce debido a las diferencias en los mecanismos de polarización de las moléculas de cada tipo de dieléctrico. De hecho, el mecanismo de polarización resulta ser un aspecto extremadamente importante en el estudio de las propiedades físicas y químicas de los dieléctricos, y en el estudio de sus propiedades eléctricas.
dieléctricos no polares
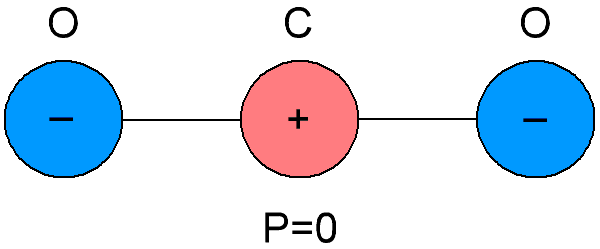
Los dieléctricos no polares también se denominan dieléctricos neutros, porque las moléculas que los componen difieren en la coincidencia de los centros de gravedad de las cargas negativas y positivas en su interior.Como resultado, resulta que las moléculas de los dieléctricos no polares no tienen su propio momento eléctrico, es igual a cero. Y en ausencia de un campo eléctrico externo, las cargas positivas y negativas de las moléculas de tales sustancias están dispuestas simétricamente.
Si se aplica un campo eléctrico externo a un dieléctrico no polar, la carga positiva y negativa de las moléculas se desplazará de su posición de equilibrio original, las moléculas se convertirán en dipolos cuyos momentos eléctricos ahora serán proporcionales a la fuerza de la corriente eléctrica. campo aplicado a ellos, y se dirigirá paralelo al campo.
Ejemplos de dieléctricos no polares que se utilizan con éxito en la actualidad como materiales aislantes eléctricos son los siguientes: polietileno, poliestireno, hidrocarburos, aceites aislantes de petróleo, etc. Además, los representantes brillantes de las moléculas no polares son, por ejemplo, nitrógeno, dióxido de carbono, metano, etc. Señor.
Los dieléctricos no polares, debido a sus bajos valores de tangente de pérdida dieléctrica, se utilizan ampliamente como dieléctricos de alta frecuencia en capacitores como el K78-2.
dieléctricos polares
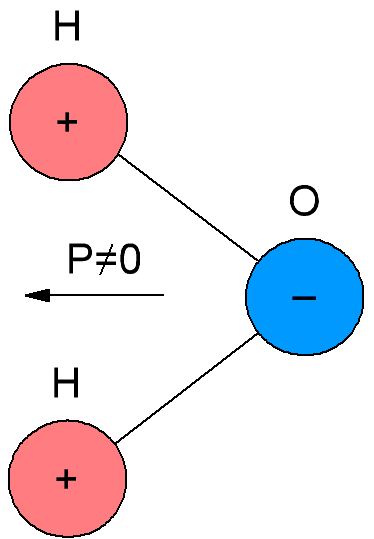
En los dieléctricos polares, también llamados dieléctricos dipolares, las moléculas tienen su propio momento eléctrico, es decir, sus moléculas son polares. La razón es que las moléculas de dieléctricos polares tienen una estructura asimétrica, por lo que los centros de masa de cargas negativas y positivas en las moléculas de dichos dieléctricos no coinciden.
Si en un polímero no polar algunos de los átomos de hidrógeno son reemplazados por átomos de otros elementos o por radicales no hidrocarbonados, entonces obtendremos solo un dieléctrico polar (dipolo), ya que la simetría se romperá como resultado de tal reemplazo. Al determinar la polaridad de una sustancia por su fórmula química, el investigador debe, por supuesto, tener una idea de la estructura espacial de sus moléculas.
Cuando no hay campo eléctrico externo, los ejes de los dipolos moleculares se orientan arbitrariamente debido al movimiento térmico, de modo que en la superficie del dieléctrico y en cada elemento de su volumen la carga eléctrica es en promedio cero. Sin embargo, cuando se introduce un dieléctrico en un campo externo, se produce una orientación parcial de los dipolos moleculares.Como resultado, aparecen cargas conectadas macroscópicamente no compensadas en la superficie del dieléctrico, creando un campo dirigido al campo externo.
Los ejemplos de dieléctricos polares incluyen los siguientes: hidrocarburos clorados, resinas epoxi y fenol formaldehído, compuestos de silicio, etc. Las moléculas de agua y alcohol, por ejemplo, también son ejemplos notables de moléculas polares. Los dieléctricos polares son ampliamente utilizados en diversos campos de la tecnología, como piezoeléctricos y ferroeléctricos, óptica, óptica no lineal, electrónica, acústica, etc.

